Page 12 - 7期
P. 12
化学专题
表 2 数字化实验“四重表征”教学
实验 物质 宏观表征 微观表征 符号表征 曲线表征
加热升温,固体 温度升高达到化合 熔融 + - 1. 上升段:温度逐渐升高,达到熔点后,
3 氯化钠 NaCl Na +Cl
熔融为液态,撤 物的熔点时,离子 开始出现电流,电流急剧上升
+
4 氯化钾 去热源后,又凝 键断开,形成了可 KCl 熔融 K +Cl - 2. 最大值:温度升高到所有化合物均
固 以自由移动的阴离 熔融 已熔融时,电流出现最大值,在这
2+
5 氯化镁 子和阳离子,在外 MgCl 2 Mg +2Cl - 一段电流出现波动的原因是熔融时
界电压的作用下定 熔融 液体沸腾产生气泡导致电流变化
2+
6 氯化钙 CaCl 2 Ca +2Cl -
向移动产生电流 3. 下降段:撤去热源后,温度逐渐降
4 熔融
2+
8 硫酸锌 ZnSO Zn +SO4 2- 低,离子减少,电阻增大,电流减小,
最终为 0 mA
+
9 氢氧化钠 NaOH 熔融 Na +OH -
1 冰醋酸 冰醋酸和水在常 化合物变为熔融状 CH 3 COOH 从开始至熔融状态,曲线都为一条直线,
温下呈熔融状 态后没有产生能够 电流传感器采集到的数据为 0 mA,此
2 水 态,氯化铝加热 使电流传感器采集 H 2 O 类物质在熔融状态下没有产生能够使电
熔融,撤去热源 到电流的阴离子和 流传感器采集到电流的自由移动的离子
7 氯化铝 后,又凝固 阳离子,不导电 AlCl 3
【学生】通过分析电流变化曲线,得出实验 2. 对不同类别化合物的电流曲线进行四重表
结论:冰醋酸、水、氯化铝在熔融状态下电流为 0 征分析
mA,氯化钠、氯化钾、氯化镁、氯化钙、硫酸锌、 【教师】“四重表征”包括“宏观表征—微观
氢氧化钠在熔融状态下产生电流,完全熔融时达到 表征—符号表征—曲线表征”。其中“曲线表征”
最大电流,随温度降低,电流逐渐减小。 是以手持实验所得曲线为分析模板,将曲线的起点、
设计意图:通过实验认识共价化合物与离子化 终点、拐点等特殊点、曲线变化趋势及不同线段与
合物在熔融状态下的不同现象,从而感性认知共价 实验现象、微粒变化和反应方程式建立联结。
键和离子键的区别。宏观感知有助于学生认识微观 【学生 】分析实验 1、2、7 的 电流 均为
本质(电子式的学习),对“物质的结构决定性质” 0 mA,所得曲线均为直线,但实验 3、4、5、6、
这一化学规律有更加深刻的认识。 8、9 中的电流均可分为上升段、最大值和下降段,
( 三 ) 分析总结,对电流曲线数据及四重表征 用“四重表征”进行分析,具体情况见表 2。
分析 【教师】通过实验可知,并不是所有的原子或
1. 曲线数据分析 原子团都以“离子键”结合,也并不是所有的离子
通过实验可得 9 条电流曲线,其中实验 1、2、 都是“离子化合物”,从而引出新概念——“共价键”
7 的电流从开始至结束都为 0 mA,实验 3、4、5、 和“共价化合物”,共价键在熔融状态下不易发生
6、8、9 的电流都先由 0 mA 逐渐升高(以氯化钠 断裂形成自由移动的离子。
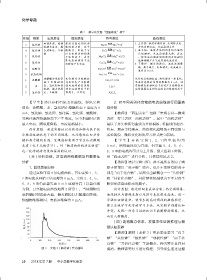
为例,其实验电流曲线如图 3 所示),当待测物完 设计意图:通过对四重表征分析,将宏观现象、
全熔融时到达最大值,撤去酒精灯后随温度降低, 曲线特点与微观本质以及符号表征联系起来,进一
熔融物渐渐凝固,电流逐渐降为 0 mA。 步强化证据意识,使学生提高对图线的敏感程度,
建立系统学习化学的学习方法。从实验中创建认知
冲突,发现一些学习过的知识不能解释的现象,从
而引入新概念。
( 四 ) 建构概念体系,发展学生证据推理与模
型认知素养
【教师】教材(必修 2)要求学生学习“离子
键”“共价键”“极性键”“非极性键”“离子化
合物”“共价化合物”等新概念,种类繁多且容易
图 3 实验 3 ( 氯化钠 ) 变化曲线 混淆,教师需要对其进行梳理,引导学生通过证据
10 2018 年第 7 期 中小学数字化教学
௹ JOEE ༯